Ung thư tiền liệt tuyến, nguyên lý nội khoa
Tin liên quan
- 10 loại rau củ bán đầy chợ Việt, là khắc tinh của ung thư (01/05/2024)
- Kỳ diệu loại rau có thể làm giảm nguy cơ mắc nhiều loại ung thư (09/05/2024)
- Phát hiện chất dinh dưỡng quan trọng trong trứng có khả năng chống lại ung thư (13/05/2024)
- Sử dụng thịt bò không đúng cách gây nguy hiểm cho sức khỏe (01/05/2024)
- Trung Quốc đột phá trong quá trình sinh tổng hợp thuốc điều trị ung thư paclitaxel (16/05/2024)
Nhận định chung ung thư tiền liệt tuyến
Ung thư tiền liệt tuyến được chấn đoán trong 241,740 đàn ông năm 2012 ở Mỹ-Tỷ lệ này có thể tương đương với ung thư vú. Khoảng 28,170 nam giới ch*t do ung thư tiền liệt tuyến năm 2012. Chẩn đoán sớm ung thư ở nam giới có triệu chứng nhẹ phát hiện qua sàng lọc có tăng nồng độ PSA trong huyết tương điều trị rất phức tạp. Giống như phần lớn các loại ung thư khác, ảnh hưởng chủ yếu liên quan đến tuổi. Bệnh thường gặp ở người da đen hơn da trắng. Các triệu chứng thường tương tự và có thể không phân biệt được với phì đại tuyến tiền liệt, nhưng những bệnh nhân bị ung thư thường có bí đái và đau lưng hoặc đau hông. Trên mô học, 95% là ung thư biểu mô tuyến. Tiên lượng phụ thuộc vào độ mô học (thang điểm Gleason).
Đối lập với tăng sinh tuyến tiền liệt, ung thư tuyến tiền liệt thường có nguồn gốc từ vùng ngoại vi của tuyến và có thể phát hiện được qua thăm trực tràng (DRE) biểu hiện bằng một hoặc nhiều nốt ở mặt sau của tuyến, khối rắn ít di động và hình dạng bất thường. Tiếp cận chẩn đoán được chỉ ra ở Hình. Những bệnh nhân có DRE âm tính và PSA ≤ 4 ng/mL có thể được theo dõi hàng năm. Những bệnh nhân có bất thường DRE hoặc PSA >10 ng/mL nên siêu âm tuyến tiền liệt qua trực tràng (TRUS). Những bệnh nhân có DRE bình thường và PSA từ 4.1–10 ng/mL được xử lý khác nhau ở các trung tâm khám chữa bệnh khác nhau.
Một số trung tâm tiến hành TRUS và sinh thiết bất kì bất thường nào hoặc tiếp tục theo dõi nếu không phát hiện ra bất thường. Một số khác nên xét nghiệm lại PSA mỗi một năm và sinh thiết nếu mỗi gian đoạn tăng > 0.75 ng/mL. Các phương pháp khác của PSA để phân biệt ung thư sớm với phì đại tuyến tiền liệt gồm xác định ranh giới và PSA tự do và PSA liên quan đến kích thước tuyến tiền liệt (tỷ trọng PSA). Có thể một phần ba số người ung tư tiền liệt tuyến không có tăng PSA.
Ung thư lan đến hạch bạch huyết được quyết định phẫu thuật; nó chỉ biểu hiện 10% số bệnh nhân với thang điểm Gleason dưới 5 và trong 70% số bệnh nhân với thang điểm 9 hoặc 10.
Nồng độ PSA liên quan đến sự di căn; chỉ 10% người có PSA < 10 ng/mL có di căn hạch. Xương là vị trí hay gặp di căn xa nhất. Đánh giá giai đoạn theo Whitmore-Jewett gồm A: không sờ thấy khối U; B: sờ thấy khối U ở 1 (B1) hoặc 2 (B2) thùy; C: khối U lan ra ngoài vỏ; và D: di căn xa.
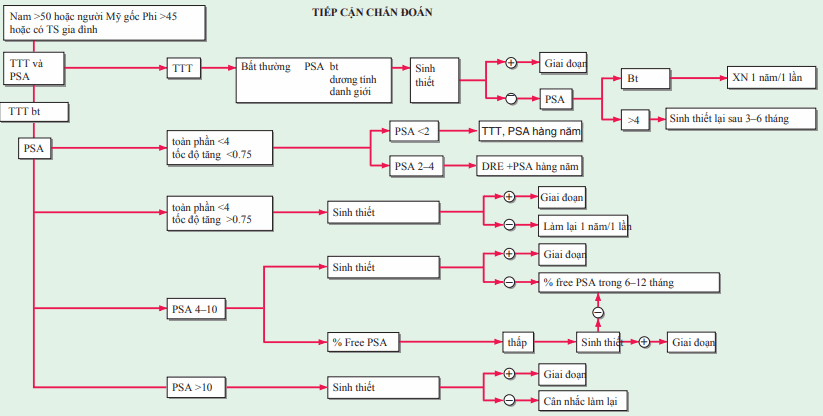
Hình. Sử dụng thăm trực tràng (TTT) và xét nghiệm PSA để quyết định sinh thiết tuyến tiền liệt dưới siêu âm.
Điều trị ung thư tiền liệt tuyến
Với ung thư giai đoạn A-C, phẫu thuật cắt tuyến tiền liệt triệt căn và xạ trị có kết quả như nhau; tuy nhiên, hầu hết các bệnh nhân được phẫu thuật. Cả 2 phương pháp đều có thể gây liệt dương. Phẫu thuật thường gây són tiểu. Xạ trị thường gây viêm trực tràng, hậu môn có thể có chảy máu, hẹp. Điều trị hormone (goserelin) cho bệnh giai đoạn khu trú sau xạ trị cải thiện hiệu quả điều trị. Bệnh nhân phải có kì vọng sống 5 năm mới phẫu thuật triệt căn. Bệnh nhân giai đoạn A có thời gian sống như những người không mắc ung thư cùng lứa tuổi. Giai đoạn B, C có tỉ lệ sống 10 năm là 82% và 42%.
Bệnh nhân sau phẫu thuật có tăng PSA có thể chụp Prostascint scanning (kháng thể của kháng nguyên PSA). Nếu không thấy bất thường, bệnh nhân được theo dõi tiếp. Nếu thấy bất thường ở giường tuyến tiền liệt, bệnh đã tái phát tại chỗ và cần xạ trị ngoài vào vị trí đó (nếu bệnh nhân đã điều trị bằng xạ trị, có thể điều trị phẫu). Tuy nhiên, trong hầu hết các trường hợp, PSA tăng sau điều trị cho thấy bệnh đã lan toàn thân. Điều trị ở giai đoạn này chưa rõ hiệu quả.
Với bệnh nhân đã đi căn xa, điều trị ức chế sản xuất androgen là 1 lựa chọn. Phẫu thuật cắt tinh hoàn có hiệu quả, nhưng hầu hết bệnh nhân thích dùng Thu*c leuprolide, 7.5 mg tiêm bắp hàng tháng (ức chế sản xuất hormone hướng Sinh d*c từ tuyến yên), với flutamide, 250 mg uống 3 lần/ngày (ức chế receptor androgen). Hiệu quả của phối hợp với flutamide vẫn còn bàn bãi. Các phương pháp khác gồm cắt tuyến thượng thận, cắt tuyến tùng, dùng estrogen, Thu*c ức chế tuyến thượng thận aminoglutethimide. Thời gian sống trung bình với giai đoạn D là 33 tháng. Khối U đôi khi đáp ứng với liệu pháp giảm hormone bằng cách co lại. Phương pháp ức chế hormone thứ hai là ức chế sản xuất androgen tại khối U; abiraterone, ức chế CYP17 ngăn cản tổng hợp androgen và MDV3100, 1 chất kháng androgen, cải thiện khả năng sống. Nhiều trường hợp bệnh vẫn tiến triển khi điều trị ức chế hormone là những khối U không phụ thuộc androgen thường liên quan đến đột biến gen mã hóa receptor androgen và làm khối U kháng Thu*c. Hóa trị nhằm mục đích điều trị giảm nhẹ trong ung thư tuyến tiền liệt.
Mitoxantrone, estramustine, và taxanes, đặc biệt là cabazitaxel, dường như có hiệu quả khi dùng đơn độc, phác đồ phối hợp thuộc đang được thử nghiệm. Bệnh nhân được hóa trị thường giảm đau nhiều hơn so với những bệnh nhân chỉ chăm sóc hỗ trợ tại nhà. Liệu pháp ức chế miễn dịch đặc hiệu cải thiện thời gian sống thêm 4 tháng ở những bệnh nhân kháng với liệu pháp ức chế hormone.
Đau xương do di căn xương có thể giảm nhẹ với strontium-89 hoặc samarium-153. Bisphosphonate giảm tỉ lệ gặp biến chứng về xương.
Dự phòng ung thư tiền liệt tuyến
Finasteride và dutasteride giảm 25% tỉ lệ mới mắc ung thư, không có hiệu quả trong cải thiện thời gian sống thêm. Ngoài ra, khối U dường như có tiến triển đến giai đoạn có điểm Gleason cao hơn.
Tin liên quan
- 4 loại ung thư thường gặp ở phụ nữ và cách phát hiện sớm (19/04/2024)
- 5 bài tập sẽ giúp bạn đỡ khó chịu hơn trong thời kỳ đèn đỏ (26/04/2024)
- Lò vi sóng phát ra bao nhiêu bức xạ? Hâm nóng thức ăn bằng lò vi sóng không chỉ độc hại mà còn gây ung thư? Sự thật là gì (16/04/2024)
- Nga nghiên cứu và thu được các chất sinh học mới có khả năng chống ung thư (01/05/2024)
- Thịt trữ trong tủ lạnh quá lâu dễ sản sinh ra chất gây hại cho cơ thể (01/05/2024)
Tin cùng chuyên mục
Tin cùng nội dung
-
Ung thư tuyến tiền liệt là một trong những loại ung thư phổ biến nhất ở nam giới. Nếu được phát hiện sớm, ung thư này thường có khả năng chữa khỏi cao.
-
Tinh hoàn là cơ quan chuyên sản xuất hormone Sinh d*c nam và tinh trùng, quan trọng cho việc sinh sản nằm trong bìu ngay dưới D**ng v*t. Mặc dù ung thư tinh hoàn là khá hiếm so với các loại ung thư khác, nó là loại ung thư phổ biến nhất ở nam giới trong độ tuổi từ 15 đến 34
-
Gần đây, kết quả tổng hợp từ các nghiên cứu trong thời gian dài chứng minh rằng thức uống có cồn cũng góp phần làm tăng nguy cơ của nhóm ung thư vùng đầu cổ.
-
Ung thư vùng đầu – cổ thường bắt nguồn từ lớp tế bào gai nằm lót trong bề mặt ẩm ướt ở vùng đầu cổ (ví dụ như trong miệng, mũi, họng), và thường phát triển thành ung thư biểu mô tế bào gai. Ung thư vùng đầu – cổ cũng có thể bắt nguồn từ các tuyến nước bọt, nhưng tương đối ít gặp. Các tuyến nước bọt chứa nhiều loại tế bào có thể ung thư hóa, vì vậy có nhiều dạng ung thư tuyến nước bọt khác nhau.
-
Khói Thuốc lá gây hại cho cả người hút lẫn không hút Thuốc.
-
Niềm vui và nụ cười nở nhiều hơn trên môi những bệnh nhi ung thư của viện Nhi Trung ương khi được nhận quà Tết từ tay Bộ trưởng Bộ Y tế Nguyễn Thị Kim Tiến chiều ngày 6/2.
-
2 công ty dược phẩm phải trả tới 6 tỉ USD do những cáo buộc che giấu nguy cơ gây ung thư bàng quang của Thuốc Actos
-
Vitamin E là chất chống ôxy hóa, có thể bảo vệ cơ thể khỏi phản ứng có hại của các gốc tự do.
-
Điều trị ung thư ảnh hưởng đến tất cả bộ phận của cơ thể, trong đó có răng miệng.
-
Ung thư tuyến giáp ở trẻ em là bướu nội tiết ác tính dạng đặc thường gặp thứ 3 và phổ biến nhất ở trẻ em.